Öz Isı ve Isı Sığası 9.Sınıf Fizik
🪄 Test ve Çalışma Kağıdı Hazırla
Konunu yaz; MEB uyumlu test ve özetler saniyeler içinde hazırlansın. 🖨️ Ücretsiz PDF indir!
- Öz Isı: 1 gram maddenin sıcaklığını 1°C ya da 1 K artırmak için gereken ısı miktarına öz ısı denir. Öz ısı, “c” sembolü ile gösterilir ve birimi cal/g°C‘dir. Öz ısısı “c” olan bir maddenin sıcaklığını “ΔT” kadar değiştirmek için gereken ısı miktarı Q = m·c·ΔT formülü ile hesaplanır. Öz ısı, maddeler için ayırt edici bir özelliktir çünkü farklı maddelerin öz ısıları farklıdır. Örneğin, denizler karalara göre geç ısınır ve geç soğur. Bunun nedeni, suyun öz ısısının karanınkinden büyük olmasıdır.
- Isı Sığası: m kütleli bir cismin sıcaklığını 1°C artırmak için gerekli ısı miktarına ısı sığası denir. Isı sığası, C = m·c formülü ile bulunur. Isı sığası maddenin kütlesine bağlı olduğu için maddeler için ayırt edici bir özellik değildir.
- Q = m·c·ΔT = C·ΔT olduğundan C = Q / ΔT formülü ile bulunur.
- Şekildeki grafiğin eğimi, maddenin ısı sığasını verir.
- Eğim = C = ΔQ / ΔT‘dir.
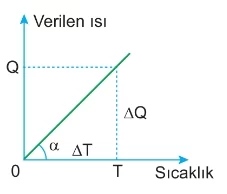
Bu formül, bir maddenin sıcaklık değişimi (ΔT) ile aldığı ya da verdiği ısı miktarı (Q) arasındaki ilişkiyi gösterir ve eğim ısı sığasını (C) verir.
İki deney tüpünden birine su, diğerine kütlesi suyunkine eşit olan zeytin yağı konulup özdeş ısıtıcılarla eşit süreler ısıtıldığında zeytin yağının sıcaklığının daha çok arttığı görülür. Eşit kütleli su ile zeytin yağına eşit ısılar verilmesine karşılık zeytin yağının sıcaklığı, suyunkinden daha çok artar. Benzer şekilde bir tencere su ile koca bir kazan su özdeş ısıtıcılarla ısıtıldığında her ikisinin de sıcaklığının aynı miktar artması için kazandaki suyun daha uzun süre ısıtılması ve daha çok ısı verilmesi gerekir.
Eşit kütleli iki maddenin sıcaklığını belirli bir miktarda yükseltmek için gereken enerji maddenin cinsine göre değişir. Aynı cins iki maddenin sıcaklığını aynı miktar yükseltmek için gereken enerji maddenin kütlesi ile doğru orantılıdır.
Eşit kütleli iki maddenin sıcaklığını belirli bir miktarda yükseltmek için gereken enerji maddenin cinsine göre değişir. Aynı cins iki maddenin sıcaklığını aynı miktar yükseltmek için gereken enerji maddenin kütlesi ile doğru orantılıdır.
Bir maddenin sıcaklığını 1°C yükseltmek için gereken enerjiye “ısı sığası” ya da “ısı kapasitesi” denir. C harfi ile gösterilir. Buna göre bir maddeye Q kadar ısı verildiğinde sıcaklığı Δt kadar artar. O halde,

Herhangi bir maddenin birim kütlesinin sıcaklığını 1°C artırmak için gereken enerjiye “öz ısı, özgül ısı” ya da “ısınma ısısı” denir ve c ile gösterilir. Kütlesi m olan bir maddeye Q kadar ısı verildiğinde maddenin sıcaklığı A1 kadar değişiyorsa maddenin özgül ısısı;
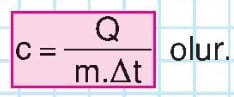
Maddeler için ayırt edici bir özelliktir. Öz ısı, bir maddenin, bu maddeye verilen enerjiye karşı ısıl duyarlılığının bir ölçüsüdür. Bir maddenin özgül ısısı ne kadar büyükse, belirli sıcaklık değişimini sağlamak için maddeye o kadar çok enerji verilmesi gerekir. m kütleli bir madde ile bu maddenin çevresi arasındaki ısı enerjisi transferi Q, maddenin sıcaklığındaki değişme miktarı Δt ise;

Bir maddeye ısı verildiğinde madde hal değiştirmemek koşuluyla maddenin sıcaklığı artar ve maddeye enerji akışı olur. Madde soğuyorsa sıcaklığı azalır ve maddeden dışarıya enerji transferi olur.
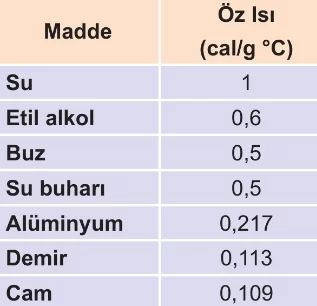
Özgül ısı, sıcaklıkla değişir. Ancak sıcaklık aralığı çok büyük değilse özgül ısıdaki değişme önemsenmez ve sabit kabul edilebilir. Tablo 2 ye dikkat edildiyse özgül ısısı en büyük olan madde su dur. Bu nedenle su geç ısınır, geç soğur. Yazın karaların denizlerden sıcak, kışın denizlerin karalardan sıcak olmasının nedeni budur.
Öz Isı ve Isı Sığası – Çözümlü Örnek Sorular
Örnek 1:
Soru: 500 gram bakırın sıcaklığını 20°C’den 80°C’ye çıkarmak için ne kadar ısı gerekir? Bakırın öz ısısı 0.385 J/g°C’dir.
Çözüm:
- Kütle (m): 500 g
- Sıcaklık farkı (ΔT): 80°C – 20°C = 60°C
- Öz ısı (c): 0.385 J/g°C
Isı miktarı formülü: Q = m * c * ΔT
Q = 500 g * 0.385 J/g°C * 60°C
Q = 11550 J
500 gram bakırın sıcaklığını 20°C’den 80°C’ye çıkarmak için 11550 joule ısı gerekmektedir.
Örnek 2:
Soru: 2 kg suyun sıcaklığını 30°C’den 90°C’ye çıkarmak için ne kadar ısı gerekir? Suyun öz ısısı 4.18 J/g°C’dir.
Çözüm:
- Kütle (m): 2 kg = 2000 g
- Sıcaklık farkı (ΔT): 90°C – 30°C = 60°C
- Öz ısı (c): 4.18 J/g°C
Isı miktarı formülü: Q = m * c * ΔT
Q = 2000 g * 4.18 J/g°C * 60°C
Q = 501600 J
2 kg suyun sıcaklığını 30°C’den 90°C’ye çıkarmak için 501600 joule ısı gerekir.
Örnek 3:
Soru: 300 gram alüminyum parçası 100°C sıcaklıktadır. Bu parçayı 25°C’ye soğutmak için kaç joule ısı gerekir? Alüminyumun öz ısısı 0.900 J/g°C’dir.
Çözüm:
- Kütle (m): 300 g
- Sıcaklık farkı (ΔT): 100°C – 25°C = 75°C
- Öz ısı (c): 0.900 J/g°C
Isı miktarı formülü: Q = m * c * ΔT
Q = 300 g * 0.900 J/g°C * 75°C
Q = 20250 J
300 gram alüminyum parçasını 100°C’den 25°C’ye soğutmak için 20250 joule ısı gerekmektedir.
Örnek 4:
Soru: 1500 gram bir demir parçası ısınarak 80°C’den 150°C’ye çıkıyor. Bu parça ısınırken kaç joule ısı almıştır? Demirin öz ısısı 0.450 J/g°C’dir.
Çözüm:
- Kütle (m): 1500 g
- Sıcaklık farkı (ΔT): 150°C – 80°C = 70°C
- Öz ısı (c): 0.450 J/g°C
Isı miktarı formülü: Q = m * c * ΔT
Q = 1500 g * 0.450 J/g°C * 70°C
Q = 47250 J
1500 gram demir parçasının sıcaklığını 80°C’den 150°C’ye çıkarmak için 47250 joule ısı gerekmektedir.
Örnek 5:
Soru: 600 gram buz, -10°C’den eriyip suya dönerek 0°C’ye ulaşmıştır. Buzu eriyene kadar ısıtmak için kaç joule ısı gerekir? Buzun öz ısısı 2.1 J/g°C ve erime ısısı 334 J/g’dir.
Çözüm:
Buzun 0°C’ye gelmesi için önce ısıtılması, sonra erimesi gerekir. Öncelikle, buzun -10°C’den 0°C’ye ısıtılması için gereken ısıyı bulalım:
- Kütle (m): 600 g
- Sıcaklık farkı (ΔT): 0°C – (-10°C) = 10°C
- Öz ısı (c): 2.1 J/g°C
Isı miktarı formülü: Q1 = m * c * ΔT
Q1 = 600 g * 2.1 J/g°C * 10°C
Q1 = 12600 J
Şimdi buzun erimesi için gereken ısıyı hesaplayalım:
Q2 = m * Le
Q2 = 600 g * 334 J/g
Q2 = 200400 J
Toplam ısı:
Qtoplam = Q1 + Q2
Qtoplam = 12600 J + 200400 J
Qtoplam = 213000 J
600 gram buzu -10°C’den 0°C’ye kadar ısıtıp tamamen eritebilmek için toplam 213000 joule ısı gerekmektedir.
Çözümlü Test Soruları 2
1. Soru: Öz ısı (özgül ısı) ile ilgili aşağıdaki ifadelerden hangisi doğrudur?
A) Bir maddenin kütlesine bağlıdır. B) Maddenin hal değişimi sırasında aldığı veya verdiği ısı miktarıdır. C) Birim kütledeki bir maddenin sıcaklığını 1°C değiştirmek için gerekli ısı miktarıdır. D) Her maddenin sıcaklığını aynı oranda artırmak için aynı miktarda ısıya ihtiyaç duymasını sağlar.
Cevap ve Çözüm:
Doğru Seçenek: C
- A) Yanlış: Öz ısı, maddenin ayırt edici bir özelliğidir ve maddenin kütlesine bağlı değildir. Bir gram suyun öz ısısı ile yüz gram suyun öz ısısı aynıdır.
- B) Yanlış: Bu ifade, gizli ısı (hal değişim ısısı) tanımına uyar. Öz ısı, hal değişimi olmadan sıcaklık değişimleri için geçerlidir.
- C) Doğru: Öz ısı (c), bir maddenin birim kütlesinin (genellikle 1 gram veya 1 kg) sıcaklığını 1°C (veya 1 Kelvin) değiştirmek için gerekli olan ısı miktarıdır. Birimi genellikle J/(g°C) veya cal/(g°C) şeklindedir.
- D) Yanlış: Farklı maddelerin öz ısıları farklı olduğu için, aynı kütledeki farklı maddelerin sıcaklığını aynı oranda artırmak için farklı miktarda ısıya ihtiyaç duyulur.
2. Soru: Aşağıdaki durumlardan hangisinde ısı sığası (ısı kapasitesi) kavramı daha ön plandadır?
A) Bir tenceredeki suyun kaynama noktasını belirlemek. B) Farklı maddelerin erime sıcaklıklarını karşılaştırmak. C) Bir termometre ile ortam sıcaklığını ölçmek. D) Aynı kütledeki demir ve bakırın sıcaklığını 10°C artırmak için gereken ısı miktarını karşılaştırmak.
Cevap ve Çözüm:
Doğru Seçenek: D
- A) Yanlış: Kaynama noktası, maddenin hal değişim sıcaklığıdır ve öz ısı veya ısı sığasıyla doğrudan ilgili değildir.
- B) Yanlış: Erime sıcaklığı, bir maddenin karakteristik bir özelliğidir ve öz ısı veya ısı sığasıyla doğrudan ilişkili değildir.
- C) Yanlış: Ortam sıcaklığını ölçmek, termometrenin çalışma prensibiyle ilgilidir.
- D) Doğru: Isı sığası (C = m ⋅ c), bir maddenin tamamının sıcaklığını 1°C değiştirmek için gerekli ısı miktarıdır. Bu durumda, aynı kütledeki farklı maddelerin (demir ve bakır gibi) farklı öz ısılara sahip olması nedeniyle, onların sıcaklıklarını belirli bir miktar artırmak için gereken ısı miktarı (ısı sığaları) farklı olacaktır. Bu karşılaştırma doğrudan ısı sığası kavramıyla ilgilidir.
3. Soru: Eşit kütledeki K ve L sıvılarının sıcaklıkları eşit miktarda artırılmak isteniyor. Eğer K sıvısının öz ısısı L sıvısının öz ısısından daha büyükse, bu durumla ilgili aşağıdakilerden hangisi doğrudur?
A) K sıvısına verilen ısı miktarı L sıvısına verilen ısı miktarından azdır. B) L sıvısına verilen ısı miktarı K sıvısına verilen ısı miktarından fazladır. C) Her iki sıvıya da aynı miktarda ısı verilmesi gerekir. D) K sıvısına verilen ısı miktarı L sıvısına verilen ısı miktarından fazladır.
Cevap ve Çözüm:
Doğru Seçenek: D
- Isı değişimi formülü şeklindedir.
- Soruda kütleler (m) eşit, sıcaklık değişimleri () eşit.
- K sıvısının öz ısısı () L sıvısının öz ısısından () daha büyükse (), o zaman K sıvısına verilmesi gereken ısı miktarı () L sıvısına verilmesi gereken ısı miktarından () daha fazla olacaktır. Çünkü aynı kütledeki bir maddenin sıcaklığını aynı oranda artırmak için öz ısısı büyük olana daha fazla enerji verilmesi gerekir.
4. Soru: Bir maddenin ısı sığasını artırmak için, aşağıdakilerden hangisi yapılmalıdır?
A) Maddenin öz ısısını azaltmak B) Maddenin kütlesini azaltmak C) Maddenin kütlesini artırmak D) Maddenin sıcaklığını artırmak
Cevap ve Çözüm:
Doğru Seçenek: C
- Isı sığası (C) formülü şeklindedir, burada m kütle, c ise öz ısıdır.
- A) Yanlış: Öz ısıyı azaltmak, ısı sığasını da azaltır.
- B) Yanlış: Kütleyi azaltmak, ısı sığasını azaltır.
- C) Doğru: Formülden de görüldüğü gibi, maddenin kütlesini artırmak, ısı sığasını artırır.
- D) Yanlış: Maddenin sıcaklığını artırmak, o anki ısı miktarını artırır ancak ısı sığasını (yani 1°C sıcaklık değişimi için gereken ısıyı) değiştirmez. Isı sığası maddenin kütlesi ve öz ısısına bağlıdır.
5. Soru: Denizlerin karalara göre geç ısınıp geç soğumasının temel nedeni nedir?
A) Deniz suyunun kütlesinin çok fazla olması B) Deniz suyunun öz ısısının karalara göre daha büyük olması C) Denizlerin derinliğinin fazla olması D) Denizlerdeki akıntıların varlığı
Cevap ve Çözüm:
Doğru Seçenek: B
- A) Yanlış: Kütlenin fazla olması bir etkendir ancak temel neden değildir. Öz ısı, maddenin ayırt edici bir özelliğidir ve ana faktördür.
- B) Doğru: Suyun öz ısısı, karayı oluşturan kayaçların ve toprakların öz ısısından çok daha büyüktür. Yani, suyun sıcaklığını 1°C artırmak için karadan çok daha fazla ısı enerjisi gerekir. Bu nedenle, aynı miktarda ısı aldıklarında karalar suya göre daha çabuk ısınır, aynı miktarda ısı verdiklerinde ise daha çabuk soğur. Bu durum, deniz kenarındaki yerleşim yerlerinde sıcaklık farklarının daha az olmasına neden olur.
- C) Yanlış: Derinlik bir etken olsa da, temel neden öz ısı farkıdır.
- D) Yanlış: Akıntılar yerel sıcaklık dağılımını etkileyebilir ancak karaların ve denizlerin genel ısınma/soğuma prensibini açıklamaz.
BİTTİİİİİ AMA BENDE BİTTİMMMMMMM
Süper olmuş performansımda çok işime yaradı teşekkürler.