London Kuvveti 9. Sınıf Kimya
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
Kimyasal bağlar ve moleküller arasındaki etkileşimler, maddelerin fiziksel özelliklerini belirlemede kritik öneme sahiptir. London kuvveti (ya da dağılma kuvvetleri), tüm moleküller arasında bulunan en zayıf çekim kuvvetlerinden biridir. Özellikle apolar moleküller arasında görülür ve geçici dipollerin oluşması sonucu meydana gelir. London kuvvetleri, moleküllerin bir arada kalmasını sağlayan temel etkileşimlerden biridir.
London kuvvetleri (indüklenmiş dipol – indüklenmiş dipol etkileşimleri)
Moleküllerdeki atomların elektronlarının hareketleri sonucunda anlık dipoller oluşur. Bu anlık dipollere sahip moleküller arasındaki çekim kuvvetlerine London kuvvetleri denir.
Soy gazların H2, Cl2, O2, CO2 ve CH4 gibi apolar moleküllerin sıvı hâllerinde London kuvvetleri görülür.
London kuvvetleri diğer Van der Waals çekim kuvvetlerinden çok daha zayıftır. Bu nedenle bu maddelerin kaynama noktaları düşüktür.
London kuvvetlerinin gücü,
* Molekül ağırlığı arttıkça artar.
* Temas yüzeyi arttıkça artar.
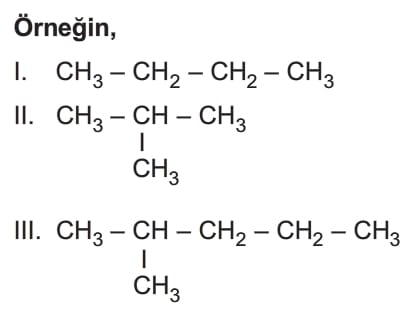
bileşiklerinin aynı ortamdaki kaynama noktalarının arasında ki ilişki III > I > II’dir.
Çünkü; III. bileşiğin molekül ağırlığı ve temas yüzeyi en büyük olduğundan London kuvveti en büyüktür. I. ve II. bileşiğin molekül ağırlıkları aynıdır ancak I. bileşiğin temas yüzeyi daha fazla olduğundan London kuvveti daha büyüktür.
Çözümlü Örnek Sorular
Soru 1
London kuvveti hangi moleküller arasında oluşur?
A) Sadece polar moleküller
B) Sadece apolar moleküller
C) Hem polar hem de apolar moleküller
D) Sadece iyonik moleküller
Çözüm:
London kuvvetleri, tüm moleküller arasında oluşabilir, ancak genellikle apolar moleküller arasındaki etkileşim olarak bilinir. Hem polar hem de apolar moleküller arasında görülebilir.
Doğru cevap: C
Soru 2
London kuvvetlerinin oluşum nedeni nedir?
A) Moleküller arası geçici dipoller
B) Moleküller arası kalıcı dipoller
C) Moleküller arasındaki iyonik bağlar
D) Moleküller arasındaki kovalent bağlar
Çözüm:
London kuvvetleri, moleküller arasında oluşan geçici dipoller sonucunda ortaya çıkar. Elektronların hareketi nedeniyle moleküllerde anlık kutuplaşmalar meydana gelir.
Doğru cevap: A
Soru 3
Aşağıdaki maddelerden hangisi London kuvvetlerinin etkisiyle bir arada tutulur?
A) H2O
B) O2
C) NaCl
D) HF
Çözüm:
O2 gibi apolar moleküller, London kuvvetlerinin etkisiyle bir arada tutulur. Diğer seçenekler, polar moleküller ya da iyonik bileşiklerdir.
Doğru cevap: B
Soru 4
London kuvvetlerinin kuvveti hangi faktöre bağlı olarak artar?
A) Molekül kütlesi
B) Molekülün polaritesi
C) Sıcaklık
D) İyon yükü
Çözüm:
Molekül kütlesi arttıkça, elektron bulutunun büyüklüğü ve dolayısıyla London kuvvetlerinin şiddeti de artar.
Doğru cevap: A
Soru 5
London kuvvetleri aşağıdaki durumların hangisinde daha güçlüdür?
A) Küçük ve hafif moleküller arasında
B) Büyük ve ağır moleküller arasında
C) Sadece iyonlar arasında
D) Polar moleküller arasında
Çözüm:
London kuvvetleri, büyük ve ağır moleküller arasında daha güçlüdür, çünkü bu tür moleküllerin elektron bulutları daha kolay kutuplaşabilir.
Doğru cevap: B

Cok tesekur ederiz
london kuvvetlerinin büyüklüğü
Teşekkürler çok güzel anlatılmış.
Güzel anlatılmış elinize sağlık