Kalıcı ve Geçici Dipol 9.Sınıf Kimya
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
Kalıcı ve İndüklenmiş Dipol Kavramları
HF, HCI ve HBr gibi polar moleküllerde, molekülü oluşturan atomların elektronegatiflikleri farklı olduğundan ![]() kutuplar oluşur.
kutuplar oluşur.
![]()
H20, OF2 ve SO2 gibi polar moleküllerde, molekülü oluşturan atomların elektronegatiflikleri farklı olduğundan ![]() kutuplar oluşur.
kutuplar oluşur.
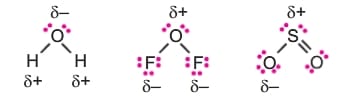
Bu şekilde polar yapıya sahip olan moleküllerde yük dağılımı simetrik değildir. Bu tür moleküllerde kalıcı dipol vardır.
H2, O2 ve F2 gibi moleküller apolar bağ içeren, apolar moleküllerdir.
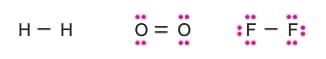
CO2, BF3 ve CH4 gibi moleküller, polar bağ içeren apolar moleküllerdir.
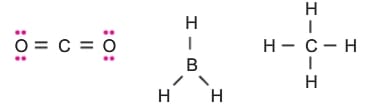
Bu şekilde apolar yapıya sahip olan moleküllerde yük dağılımı simetriktir. Elektronlar sürekli hareketli olduklarından bu simetrik yük dağılımlarında anlık değişmeler meydana gelir. Böylece elektron yoğunluklarının farklı olmasıyla anlık (geçici) dipoller oluşur. Bu şekilde ortaya çıkan dipollere indüklenmiş dipol denir.