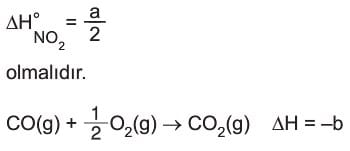Oluşum Entalpisi 11. sınıf kimya
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
Standart şartlarda (25°C, 1 atm) elementlerden başlayarak bileşiklerin oluşumu sırasında meydana gelen enerji değişimine standart oluşum entalpisi denir. Oluşum entalpileri Hf0 veya H0 ile gösterilir. Tepkimenin elementlerden başlamasının nedeni standart şartlarda elementlerin oluşma entalpilerinin sıfır kabul edilmesidir. Örneğin standart şartlarda suyun oluşum tepkimesinin entalpisi,
MOLAR OLUŞUM ISISI
Standart koşullarda bir mol bileşiğin elementlerinden oluşumu sırasında meydana gelen ısı değişimine molar oluşum ısısı veya molar oluşma entalpisi denir.
BİLGİ: Oluşma entalpisine bakılırken karbonun allotroplarından C(grafit) standart alınır. Örneğin elmasın yakılması sırasında çıkan ısı CO2 gazının molar oluşum ısısı değildir. Ayrıca oksijenin allotroplarından oksijen gazı (O2) standart kabul edilir. Molar oluşum entalpisinde oluşan ürünün katsayısının “1″ olmasına ve girenlerin element olmasına dikkat edilmelidir.
Tepkimeye girenler element olsa da üründen 2 mol NO2 gazı oluştuğu için a değeri NO2 nin molar oluşma entalpisi değildir. NO2 gazının molar oluşma entalpisi,
Bu tepkimenin entalpi değeri de CO2 gazının molar oluşma entalpisi değildir; çünkü girenlerde bileşik vardır. Bu tepkimenin entalpisine CO gazının molar yanma entalpisi denir.
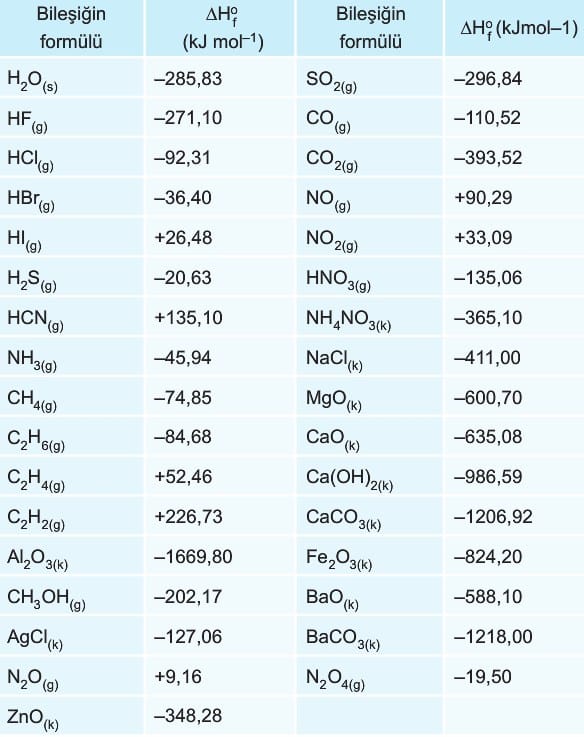
Aşağıdaki tabloda bazı maddelerin standart oluşum entalpileri verilmiştir.
TEPKİME ENTALPİLERİNİN HESAPLANMASI
Oluşma Entalpilerinden Tepkime Entalpisinin Hesaplanması
Tepkime entalpisini hesaplarken ürünlerin toplamı oluşma entalpilerinden girenlerin toplam oluşma entalpileri çıkartılır.
BİLGİ: Tepkime entalpilerinde kullanılan (-) veya (+) işaret tepkime ısının yönünü belirtmek içindir. Bir büyüklük göstergesi değildir. Eğer soruda ne kadar ısı çıkar veya ısı gerekir deniyorsa, yön belirttiği için bulunan değer pozitif işaretlidir.
Molar Tepkime Entalpisi
Herhangi bir tepkimede “molar” ifadesi kullanılmış ise bir mol maddenin tepkimeye girdiğini gösterir. Eğer tepkime yanma tepkimesi ise molar yanma, nötralleşme tepkimesi ise molar nötrleşme ısısı olarak ifade edilir.
1. Molar Yanma Entalpisi
1 mol maddenin yanması sırasında alınan ya da verilen ısıya molar yanma entalpisi denir. N2 yanması hariç tüm yanma tepkimeleri ekzotermiktir.
2. Molar Nötralleşme Isısı
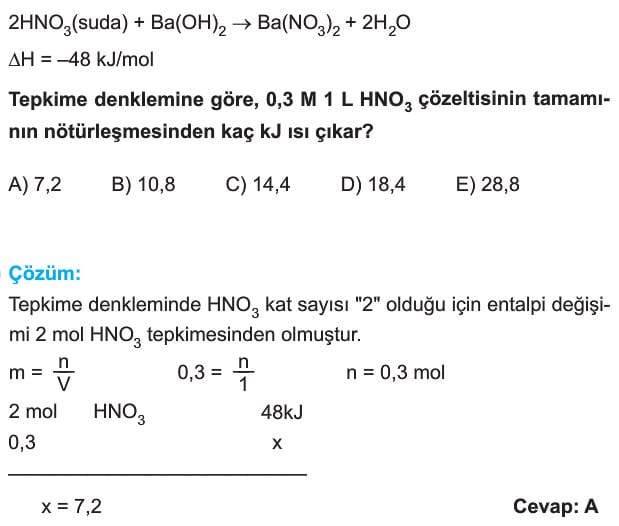
1 mol asit veya bazın nötralleşmesi sırasında açığa çıkan ısı miktarına molar nötralleşme ısısı denir. Nötralleşme tepkimeleri ekzotermiktir.
Çözümlü Örnek Test Soruları
Oluşum Entalpisi
Bir bileşiğin oluşum entalpisi, standart koşullar altında, elementlerinden bir mol bileşiğin oluşması sırasında açığa çıkan veya soğurulan ısıdır. Bu değer, bileşiklerin termokimyasal hesaplamalarında kullanılır.
1. CO₂(g) bileşiğinin oluşum entalpisi -393,5 kJ/mol’dür. Buna göre, aşağıdakilerden hangisi doğru bir yorumdur?
A) CO₂’nin oluşumu ekzotermiktir ve ısı açığa çıkar.
B) CO₂’nin oluşumu endotermiktir ve ısı soğurur.
C) CO₂’nin oluşumu sırasında enerji harcanır.
D) CO₂ oluşumu tepkimesi ısı gerektirir.
Çözüm: Negatif bir oluşum entalpisi değeri (-393,5 kJ/mol), oluşumun ekzotermik olduğunu ve ısı açığa çıktığını gösterir. Cevap A.
2. Aşağıdaki bileşiklerden hangisinin oluşum entalpisi sıfırdır?
A) O₂(g)
B) H₂O(l)
C) CO₂(g)
D) CH₄(g)
Çözüm: Elementlerin standart durumlarındaki entalpileri sıfır olarak kabul edilir. Bu nedenle, saf elementler olan O₂(g) ve H₂(g) gibi maddelerin oluşum entalpisi sıfırdır. Cevap A.
3. Bir bileşiğin standart oluşum entalpisi hakkında aşağıdaki ifadelerden hangisi doğrudur?
A) Sadece endotermik tepkimeler için hesaplanır.
B) Bileşiğin elementlerinden oluşumu sırasında açığa çıkan veya soğurulan enerjidir.
C) Her zaman pozitif bir değerdir.
D) Sadece gaz fazındaki maddeler için hesaplanır.
Çözüm: Standart oluşum entalpisi, bir bileşiğin elementlerinden oluşumu sırasında açığa çıkan veya soğurulan enerji miktarıdır. Cevap B.
4. H₂(g) + 1/2 O₂(g) → H₂O(l) tepkimesinin entalpi değişimi -286 kJ/mol olarak verilmiştir. Bu tepkimenin standart oluşum entalpisi hakkında ne söylenebilir?
A) 286 kJ/mol ısı açığa çıkar ve reaksiyon ekzotermiktir.
B) Reaksiyon endotermiktir ve 286 kJ/mol enerji soğurur.
C) Bu bir endotermik reaksiyon olup enerji gerektirir.
D) Reaksiyon sırasında hiçbir ısı değişimi olmaz.
Çözüm: Reaksiyon sırasında -286 kJ/mol ısı açığa çıkar, bu da tepkimenin ekzotermik olduğunu gösterir. Cevap A.
5. NH₄Cl(s)’nin çözünmesi endotermik bir olaydır. Çözünme sırasında ne gözlenir?
A) Çözünme sırasında ısı açığa çıkar.
B) Çözünme sırasında çevreden ısı soğurulur.
C) Çözünme sırasında sıcaklık artar.
D) Çözünme sırasında enerji açığa çıkmaz.
Çözüm: Endotermik tepkimelerde çevreden ısı soğurulur. NH₄Cl(s)’nin çözünmesi sırasında çevreye enerji verilmez, aksine soğurulur. Cevap B.
6. Standart oluşum entalpisi tablosunda olmayan bir madde için hangi yöntemle entalpi değişimi hesaplanabilir?
A) Hess yasası kullanılarak
B) Maddenin çözünme entalpisine bakılarak
C) Madde saf bir element olduğu için hesaplama yapılmaz
D) Maddenin yoğunluğu kullanılarak
Çözüm: Eğer bir maddenin standart oluşum entalpisi bilinmiyorsa, Hess yasası kullanılarak tepkimenin toplam entalpisi hesaplanabilir. Cevap A.