Isı ve Sıcaklık Nedir 9.Sınıf Fizik
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
Günlük hayatta sık kullandığımız ısı ve sıcaklık kavramları. fizikte farklı anlamdadır. Isı ve sıcaklık kavramlarının farkını anlamak için iç enerji kavramının bilinmesi gereklidir.
Bir maddenin tanecikleri iki tür enerjiye sahiptir. Bunlardan biri, tanecikler arası bağlarda depo edilen enerjidir. Bu bir tür potansiyel enerjidir. Örneğin su molekülleri arasındaki enerji, bu tür enerjidir. Burada kastedilen bağların, suyu oluşturan hidrojen ve oksijen arasındaki kimyasal bağlar olmadığına dikkat ediniz. Taneciklerin sahip olduğu diğer enerji türü, taneciklerin hareketlerinden (titreşimlerinden) kaynaklanan kinetik enerjileridir. İşte bir maddenin iç enerjisi, taneciklerinin sahip olduğu bu enerjilerin toplamıdır. Başka bir ifadeyle iç enerji, taneciklerin kinetik ve potansiyel enerjileri toplamıdır.
Sıcaklık ise madde taneciklerinin ortalama hareket enerjileri ile orantılı bir büyüklüktür. K maddesinin L den daha sıcak olması, K nin taneciklerinin ortalama hareket enerjilerinin L nin kinden büyük olması demektir.
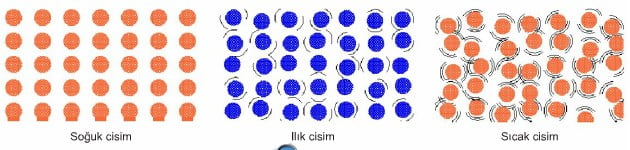
Atomların sıcaklıklarına göre titreşim hareketleri şekildeki gibi tasvir edildiğinde sıcaklığı artan cismin tanecikleri daha çok titreşir.
Soğuk su bulunan bir kaba sıcak su konulacak olursa ne olur? Soğuk suyun sıcaklığı artar, sıcak suyun sıcaklığı azalır. Soğuk suyun sıcaklığı yani moleküllerinin kinetik enerjisi artarken sıcak suyun sıcaklığı yani moleküllerinin kinetik enerjisi azalır. Böylece sıcak sudan soğuk suya enerji aktarımı yapılmış olur.
Bu şekilde belirli sıcaklıktaki bir sistemden daha düşük sıcaklıktaki bir sisteme sıcaklık farkı nedeniyle aktarılan enerji türüne ısı denir. Başka bir ifadeyle soğuk suyun sıcaklığını artıran, sıcak sudan gelen ısı enerjisidir. Öyleyse ısı enerjisi, maddenin sıcaklığını ve dolayısıyla taneciklerinin kinetik enerjilerini değiştiren enerjidir.
Bir buzu eritmek için de enerji verilir. Buz erirken sıcaklık değişir mi? Buz erirken buzun sıcaklığı 00C ve buz eriyene kadar sıcaklık 00C olarak kalır. Buza verilen enerji, tanecikler arası bağlarda depo edilen potansiyel enerjiyi artırır. Öyleyse ısı, maddenin iç enerjisinde değişime sebep olan enerjidir. Isı bir enerji türü olduğu için birimi joule ya da kaloridir. Joule ve kalori arasındaki ilişki 1 cal = 4,18 joule şeklindedir.
Bir maddenin sıcaklığı madde miktarına bağlı değildir Ama iç enerjisi madde miktarı ile doğru orantılıdır. İç enerji ölçülemez ama sıcaklık termometre ile ölçülür. Isıyı da doğrudan ölçen bir alet yoktur. Ancak ısıyı hesaplama yoluyla ölçmeye yarayan ve kalorimetre adı verilen düzenekler vardır.
Isı ve Sıcaklık Arasındaki Farklar:
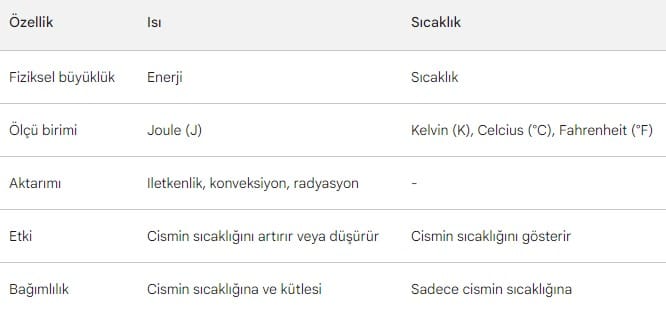
Maddeler arasında sadece sıcaklık farkı nedeniyle alınıp verilen enerjiye ısı denir. Bir madde Isı alırsa iç enerjisi artar, ısı verirse iç enerjisi azalır. Isı, sıcaklık farkı nedeniyle aktarılan enerji türü olduğundan bir maddenin ısısı olmaz.

Sıcaklıkları T, 2T olan şekildeki K ve L cisimleriyle ilgili olarak K nın ısısı L nin ısısından küçüktür ya da büyüktür gibi bir yargıda bulunulamaz.