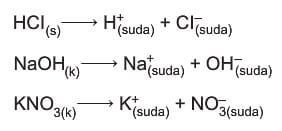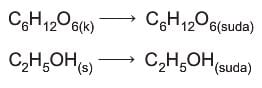Çözeltilerin Sınıflandırılması 10. Sınıf
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
Çözeltiler, çözünen maddenin çözücü içindeki oranına göre, doymuşluk durumuna göre ve elektrik iletkenliğine göre sınıflandırılabilir.
a) Çözünen Miktarına Göre Çözeltiler
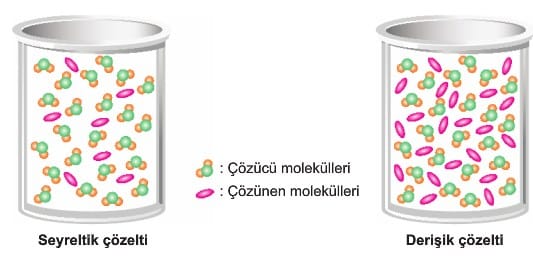
Çözünen maddenin çözücü içindeki oranına göre çözeltiler seyreltik çözelti ve derişik çözelti olarak sınıflandırılırlar. İçinde aynı miktarda su bulunan iki kap olsun. Bu kaplardan birinde 1 gram şeker çözerken diğerinde 10 gram şeker çözelim. Oluşan çözeltilerden 1 gram şeker çözünmüş olanı seyreltik, 10 gram şeker çözünmüş olanı derişik çözeltidir.
Seyreltik Çözelti
Bir çözelti içinde çözünen madde miktarı az ise bu çözeltiye seyreltik çözelti denir. Yani Çözünen/Çözücü oranı küçüktür.
Derişik çözelti
Bir çözelti içinde çözünen madde miktarı fazla ise bu çözeltiye derişik çözelti denir. Yani Çözünen/Çözücü oranı büyüktür.
b) Doymuşluk Durumuna Göre çözeltiler
Bazı maddeler birbiri içinde sonsuz oranda çözünebilirken, bazı çözeltilerde çözücü, belirli oranda madde çözebilir. Doymuşluk durumuna göre çözeltiler; doymamış çözelti, doymuş çözelti ve aşırı doymuş çözelti olarak sınıflandırılır.
Doymamış Çözelti
Belirli sıcaklıkta, çözebileceğinden daha az çözünen maddeyi çözmüş olan çözeltiye doymamış çözelti denir. Aynı sıcaklıkta, doymamış çözeltiye aynı çözünen maddeden eklenirse çözelti doygun hale gelinceye kadar çözünme devam eder ve çözünme süresince çözeltinin derişimi (çözünen/çözücü oranı) artar.
Doymuş çözelti
Belirli sıcaklıkta, çözebileceği kadar çözünen maddeyi çözmüş olan çözeltiye doymuş çözelti denir. Aynı sıcaklıkta, doymuş çözeltiye aynı çözünen maddeden eklenirse çözünme çözünen olmaz ve çözeltinin derişimi (çözünen/çözücü oranı) değişmez.
Aşırı Doymuş çözelti
Çözebileceğinden daha fazla çözünen maddeyi çözmüş olan çözeltiye aşırı doymuş çözelti denir. Aşırı doymuş bir çözelti örneğin KNO3 çözeltisi şu şekilde hazırlanabilir: Önce belirli bir sıcaklıkta doymuş KNO3 çözeltisi hazırlanır. Daha sonra çözelti ısıtılır. Çözelti ısıtıldığında daha fazla KNO3 çözünür. Bu çözelti soğumaya bırakıldığında ve ilk sıcaklığa dönüldüğünde fazladan çözünen KNO3‘ün çökmediği görülür. İşte bu çözelti aşırı doymuş bir çözeltidir. Aşırı doymuş çözelti kararsızdır. Basit bir etkiyle (sallanırsa ya da çözünen eklenirse) fazladan çözünen madde dibe çöker.
c) Elektrik İletkenliğine Göre Çözeltiler
Elektrik iletkenliğine göre çözeltiler, elektrolit çözeltiler ve yalıtkan çözeltiler olarak sınıflandırılırlar.
Elektrolit çözeltiler
Elektrik akımını ileten çözeltilere elektrolit çözeltiler denir. Suda iyonlaşarak çözünen maddelerin çözeltileri elektrik akımını iletir. Bir çözeltinin elektrik akımını iletebilmesi için o çözeltinin iyon içermesi gerekir. çözeltinin birim hacmindeki iyon sayısı (iyon sayısı / hacim) arttıkça çözeltinin elektrik iletkenliği de artar. Asit çözeltileri, baz çözeltileri ve iyonik bileşiklerin çözeltileri iyon içerdikleri için elektrolit çözeltilerdir.
Yalıtkan çözeltiler
Elektrik akımını iletmeyen çözeltilere yalıtkan çözeltiler denir. Suda moleküler olarak çözünen maddelerin çözeltileri elektrik akımını iletmez. Şeker (C6H12O6), etanol (C2H5OH) gibi suda iyonlaşmadan molekül halinde dağılan maddelerin çözeltileri yalıtkan çözeltilerdir.
Çözümlü Örnek Test Soruları
Soru 1:
Aşağıdaki çözeltilerden hangisi katı-sıvı çözeltisine örnektir?
A) Hava
B) Tuzlu su
C) Alkol-su karışımı
D) Civa-altın amalgamı
E) Gazoz
Çözüm:
Katı-sıvı çözeltilerinde katı bir madde sıvı bir çözücüde çözünür. Tuz (katı) suda (sıvı) çözünerek tuzlu su çözeltisini oluşturur.
Cevap: B
Soru 2:
I. Şekerli su
II. Kolonya
III. Alaşım
Yukarıdakilerden hangileri homojen çözeltidir?
A) Yalnız I
B) I ve II
C) II ve III
D) I, II ve III
E) Yalnız III
Çözüm:
- Şekerli su (katı-sıvı) ve kolonya (sıvı-sıvı) homojen karışımlardır.
- Alaşımlar (örneğin tunç) katı-katı homojen çözeltilerdir.
Cevap: D
Soru 3:
Aşağıdaki çözeltilerden hangisi elektrolit özellik göstermez?
A) Sirkeli su
B) Şekerli su
C) Tuzlu su
D) Asitli su
E) Soda
Çözüm:
Elektrolit çözeltiler, iyonlarına ayrışarak elektrik akımını ileten çözeltilerdir. Şeker (kovalent bileşik) suda çözündüğünde iyon oluşturmaz, bu yüzden elektrolit değildir.
Cevap: B
Soru 4:
Hava bir çözeltidir. Buna göre havanın çözücüsü ve çözüneni aşağıdakilerden hangisinde doğru verilmiştir?
A) Çözücü: Oksijen, Çözünen: Azot
B) Çözücü: Azot, Çözünen: Oksijen
C) Çözücü: Su buharı, Çözünen: Karbondioksit
D) Çözücü: Karbondioksit, Çözünen: Oksijen
E) Çözücü: Azot, Çözünen: Su buharı
Çözüm:
Hava bir gaz-gaz çözeltisidir ve en fazla bulunan bileşen (azot, %78) çözücü olarak kabul edilir. Oksijen (%21) ise çözünendir.
Cevap: B
Soru 5:
Bir çözeltinin derişik veya seyreltik olması aşağıdakilerden hangisine bağlıdır?
A) Çözücünün cinsine
B) Çözünen miktarına
C) Çözeltinin sıcaklığına
D) Çözeltinin rengine
E) Çözünenin tanecik boyutuna
Çözüm:
Derişik veya seyreltik olma durumu, birim hacimdeki çözünen madde miktarına bağlıdır.
Cevap: B