İyon Yarıçapı 9.Sınıf Kimya
🪄 Test ve Çalışma Kağıdı Hazırla
Konunu yaz; MEB uyumlu test ve özetler saniyeler içinde hazırlansın. 🖨️ Ücretsiz PDF indir!
İyon Yarıçapı
Atomlar iyonik bağlı bileşik oluşturduklarında bir iyonun çekirdeği ile diğer komşu iyonun en dış elektron bulutu arasındaki uzaklığa iyon yarıçapı denir.
Pozitif iyonların (katyonların) yarıçapları, türetildikleri metal atomlarının yarıçaplarından daha küçüktür. Çünkü, dış yörünge elektronlarının azalması, kalan elektronların her birinin çekirdek tarafından daha fazla çekilmesine neden olur. Birim elektron başına düşen çekim kuvveti artar ve bu da yarıçapın küçülmesine sebep olur.
Örneğin, nötr sodyum atomunun (Na) yarıçapı 186 pm iken, Na+ iyonunun yarıçapı 102 pm’dir. Yani, sodyum bir elektron vererek sodyum iyonuna dönüştüğünde yarıçapı küçülmüştür.
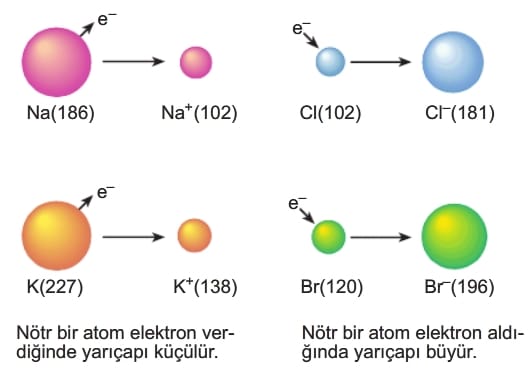
Negatif iyonların yarıçapları, türetildikleri ametal atomların yarıçaplarından daha büyüktür. Anyonlar oluşurken eklenen fazla elektron ya da elektronlar, dış orbitallerde elektronların birbirlerini itme gücünü artırır.
UYARI: Elektron sayısı aynı olan atom ya da iyonlarda proton sayısı büyük olanın atom çapı daha küçüktür.

İyon Yarıçapı -Periyodik Özelliklerin Değişimi 9.sınıf kimya
Çözüm: Bir atom ya da iyon elektron verdikçe yükü artar. Bir atom ya da iyon elektron aldıkça yükü azalır. İyonlarında ve Ne atomunda 10 ar tane elektron vardır. Taneciklerin elektron sayıları aynı olduğuna göre üçünün de elektron dizilimi 2) 8) şeklindedir. Ancak elektron dizilimlerininin aynı olması tanecik yarıçaplarının eşit olması anlamına gelmez. Atom yarıçapı çekirdeğin elektronlara uyguladığı çekim kuvveti ile ilgilidir. Buna göre çekirdekteki proton sayısı arttıkça çekirdek çekim kuvveti artar. Yani fazla protona sahip olan eşit elektronlu taneciklerde elektronlar çekirdeğe doğru daha çok çekileceğinden yarıçapı daha küçük olur.