Katılar ve Özellikleri Kimya Tyt
🪄 Test ve Çalışma Kağıdı Hazırla
Konunu yaz; MEB uyumlu test ve özetler saniyeler içinde hazırlansın. 🖨️ Ücretsiz PDF indir!
KATILAR VE ÖZELLİKLER
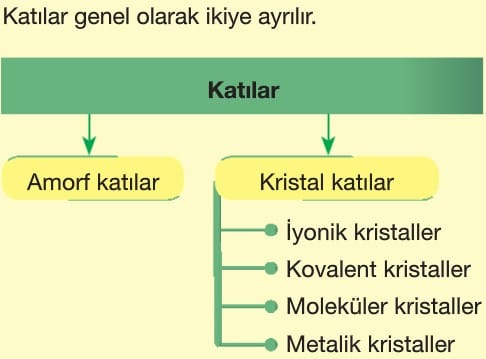
Katılar
Gaz molekülleri soğutulduğunda sıvı hale, sıvı molekülleri soğutulduklarında kinetik enerjileri azalarak daha düzenli olan katı hale geçerler. Maddenin en az potansiyel enerjili ve en düzenli haline katı hal denir.
KATILARIN GENEL ÖZELLİKLERİ
- Maddenin en az potansiyel enerjili ve en düzenli halidir.
- Belirli şekil ve hacimleri vardır.
- Tanecikler arası çekim kuvvetleri çok güçlüdür.
- Sıkıştırılamazlar.
- Sadece titreşim hareketi yaparlar.
- Isıtıldıklarında genleşirler. Genleşme katsayısı katılar için ayırt edici bir özelliktir.
AMORF KATILAR
- Katıyı oluşturan atom veya moleküller belirli bir geometrik şekle sahip değildir. Rastgele istiflenmiştir.
- Belirli bir erime noktaları yoktur.
- Serttirler ve sıkıştırılamazlar.
- Belirli sıcaklık aralıklarında yumuşarlar. Yumuşamanın başladığı bu sıcaklığa camsı geçiş sıcaklığı denir.
- Amorf katılara cam, kauçuk, plastik, tereyağı, mum gibi maddeler örnek olarak verilebilir.
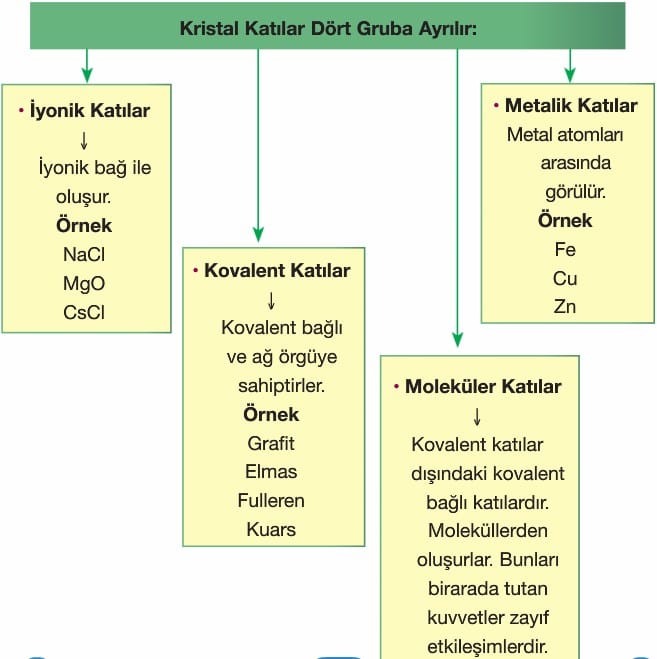
KRİSTAL KATILAR
- Katıyı oluşturan atom veya moleküller belirli bir geometrik şekle göre dizilen katılardır.
- Belirli bir sıcaklıkta erirler.
- Katıyı oluşturan tanecikler birim hücre denilen düzenli tekrar eden yapıya sahiptir.
- Serttirler ve sıkıştırılamazlar.
İyonik katılar kırılgan yapıya sahiptirler.
İyonik katılarda anyon ve katyonlar arasında elektrostatik çekim kuvvetleri olduğundan erime ve kaynama sıcaklıkları oldukça yüksektir.
İyonik katılar katı halde elektriği iletmezler, ancak erimiş halde ve suda çözündüklerinde serbest iyonlar yardımıyla elektriği iletirler.
Moleküler Katılar: Kuru buz (CO₂), kükürt (S₈), beyaz fosfor (P₄), iyot (I₂) ve buz gibi katılar moleküler yapılıdır. Bu moleküller zayıf etkileşimlerle (Van Der Waals, dipol-dipol ve hidrojen bağları) bir arada dururlar. Buzun üç boyutlu yapısında moleküller arasında hidrojen bağı etkilidir.
Moleküler Katılar: Kuru buz (CO2), kükürt (S8)beyaz fosfor (P4), iyot (I2) ve buz gibi katılar moleküler yapılıdır. Bu moleküller zayıf etkileşimlerle (Van Der Waals, dipol-dipol ve hidrojen bağları) bir arada dururlar. Buzun üç boyutlu yapısında moleküller arasında hidrojen bağı etkilidir.
Moleküller arası etkileşimler zayıf olduğundan bu katılar genellikle yumuşak, erime ve kaynama sıcaklıkları düşüktür.
Metalik Katılar: Demir, bakır, çinko, gümüş, sodyum gibi metal atomlarının serbest elektronları metal iyonları oluşturarak bu atomları bir arada tutarlar. Serbest elektronlar metallerin elektriksel iletkenliğine, parlaklık ve işlenebilirliklerine neden olurlar.
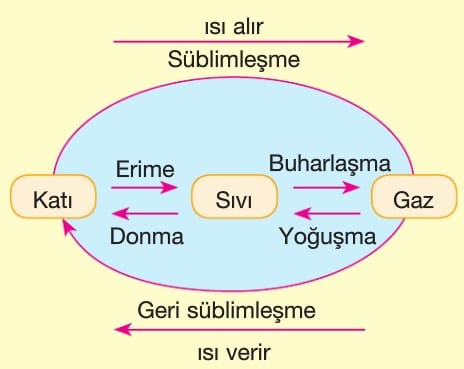
Hal Değişimleri
Maddenin ısı alarak veya vererek fiziksel halini değiştirmesidir.
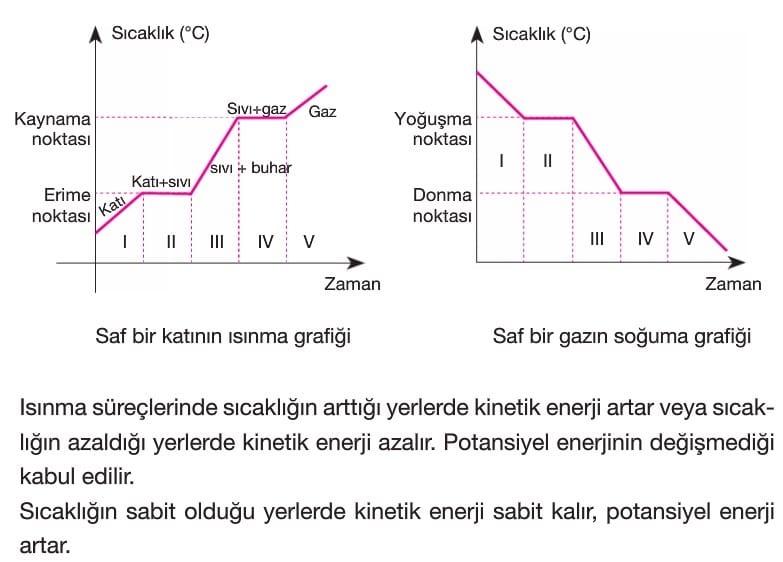
Erime: Katının ısı alarak sıvı hale geçmesidir. Sabit basınçta katı erirken sıcaklığı sabit kalır. Buna erime sıcaklığı (noktası) denir.
Donma: Sıvının ısı vererek katı hale geçmesidir. Sabit basınçta sıvı donarken sıcaklığı sabit kalır. Buna donma sıcaklığı (noktası) denir.
Saf bir maddenin erime ve donma noktası birbirine eşittir. Buz 0 oC’de erir, saf su 0 oC’de donar.
Buharlaşma: Bir sıvının ısı alarak gaz haline geçmesidir.
Yoğuşma: Bir gazın ısı vererek sıvı haline geçmesidir.
Buharlaşma ve yoğuşma birbirinin tersi olan hal değişimleridir. Bir sıvının buharlaşması için gereken ısı, aynı sıvının buharının yoğuşması sırasında açığa çıkan ısıya eşittir.
Sühlimleşme: Bir katının ısı alarak sıvılaşmadan direk gaz haline geçmesine süblimleşme, bu olayın tersine de geri süblimleşme veya kırağılaşma denir.
Örneğin; Kuru buz (katı CO2), naftalin ve iyot süblimleşme özellikleri olan maddelerdir.
Çözümlü Test Soruları
1. Aşağıdaki ifadelerden hangisi katıların genel özelliklerinden biri değildir?
A) Belirli bir şekil ve hacme sahiptirler.
B) Tanecikleri arasındaki boşluk fazladır.
C) Tanecikleri arasındaki çekim kuvveti oldukça fazladır.
D) Tanecikleri titreşim hareketi yapar.
Cevap: B (Katılar, tanecikleri arasında çok az boşluk bulunan maddelerdir.)
2. Aşağıdaki katı türlerinden hangisi amorf katılara örnektir?
A) Kuvars
B) Cam
C) Tuz
D) Elmas
Cevap: B (Cam, amorf yani düzensiz yapılı bir katıdır.)
3. Aşağıdaki katı türlerinden hangisi iyonik katılara örnektir?
A) Altın
B) Şeker
C) NaCl
D) Cam
Cevap: C (NaCl, yani sofra tuzu, iyonik bağlarla oluşmuş bir katıdır.)
4. Moleküler katılar ile ilgili aşağıdaki ifadelerden hangisi doğrudur?
A) Elektrik akımını iletirler.
B) Tanecikleri arasında güçlü iyonik bağlar bulunur.
C) Erime noktaları genellikle düşüktür.
D) Sert ve dayanıklı yapıya sahiptirler.
Cevap: C (Moleküler katılar, zayıf Van der Waals kuvvetleri ile bir arada tutulduğu için erime noktaları genellikle düşüktür.)
5. Metalik katılar ile ilgili aşağıdakilerden hangisi yanlıştır?
A) Elektrik ve ısıyı iyi iletirler.
B) Esneklik gösterirler.
C) Tanecikleri arasındaki bağlar çok zayıftır.
D) Dövülebilir ve tel haline getirilebilirler.
Cevap: C (Metalik katılar güçlü metalik bağlara sahiptir.)