Sıvıların Genel Özellikleri Kimya Tyt
🪄 Test ve Çalışma Kağıdı Hazırla
Konunu yaz; MEB uyumlu test ve özetler saniyeler içinde hazırlansın. 🖨️ Ücretsiz PDF indir!
SIVILARIN GENEL ÖZELLİKLERİ
- Sıvılar maddenin katı haline göre düzensiz, gaz haline göre daha düzenli, moleküllerin birbiri üzerinde kayabildiği hareketli halidir.
- Gazlar yeterince soğutulduklarında ve uygun basınçta sıvılaşırlar.
- Sıvıların tanecikler arası boşlukları gaza göre daha küçüktür.
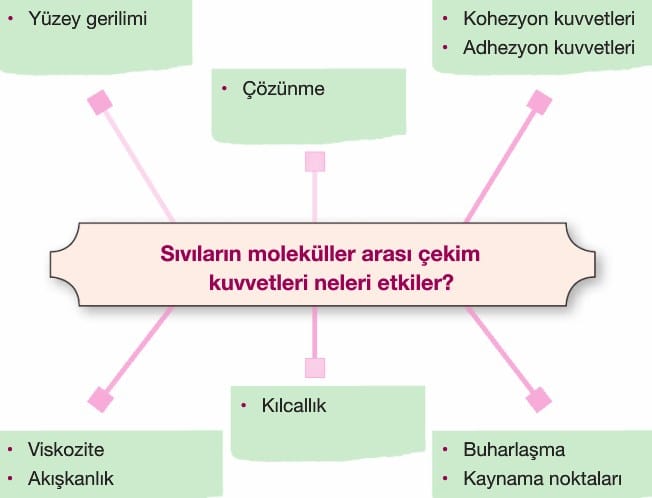
- Moleküller arası çekim kuvveti katıya göre daha az, gaza göre daha büyüktür.
- Tanecikleri arasında boşluk az olduğundan sıkıştırılamazlar.
- Belirli hacimleri olan, ancak belirli şekilleri olmayan ve konuldukları kabın bulundukları kısmının şeklini alan haldir.
- Akışkandırlar.
- Titreşim, öteleme ve dönme hareketlerini yaparlar.
Yüzey Gerilimi
Bir sıvıyı oluşturan moleküllerden birisini düşündüğümüzde bu molekül diğer moleküller tarafından her yöne eşit kuvvetle çekildiğinden net kuvvet sıfırdır. Ancak sıvı yüzeyinde bulunan bir molekül iç taraftaki moleküller tarafından çekildiğinde sıvı yüzeyi elastik bir zar gibi davranarak küresel bir hal alır ve yüzey gerilimine neden olur.
Bir sıvının yüzey alanını bir birim artırmak için gerekli olan enerjiye yüzey gerilimi denir.
Moleküller arası bağları güçlü olan sıvıların yüzey gerilimleri de genellikle büyüktür. Cıva metalik bağ içerdiğinden yüzey gerilimi en yüksek olan sıvıdır. Hidrojen bağı içeren su, etil alkol, gliserin gibi maddelerin de yüzey gerilimleri oldukça büyüktür.
Adhezyon ve Kohezyon Kuvvetleri
İki farklı maddenin molekülleri arasında oluşan çekim kuvvetine adhezyon kuvvetleri, bir maddenin kendi molekülleri arasındaki çekim kuvvetine ise kohezyon kuvveti denir.
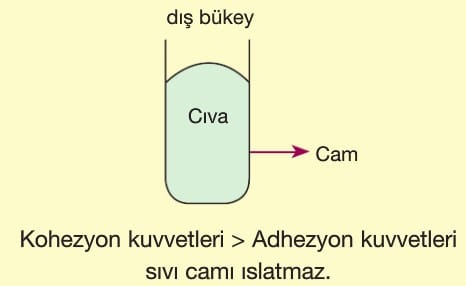
Bir sıvının bir yüzeyi ıslatması ya da ıslatmadan küresel yapısını koruması bu iki kuvvete bağlıdır.
- Bir sıvıdaki kohezyon kuvvetleri temas ettiği yüzeyden daha güçlü ise sıvı temas ettiği yüzeyi ıslatmaz. Bu durumda Kohezyon Kuvvetleri > Adhezyon kuvvetleridir.
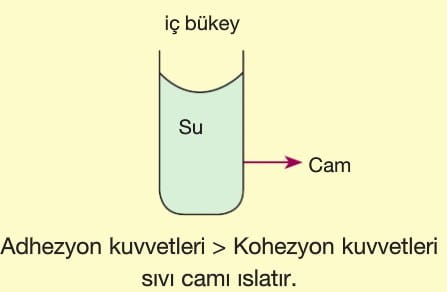
- Bir sıvının temas ettiği yüzeyle oluşan adhezyon kuvvetleri, sıvının kendi molekülleri arasındaki kohezyon kuvvetlerinden güçlü ise sıvı temas ettiği yüzeyi ıslatır. Bu durumda Adhezyon Kuvvetleri > Kohezyon kuvvetleridir.
Kılcallık (Kapiler Etki): Bir sıvının temas ettiği katı yüzeyi tarafından yükselmesi veya alçalması olayıdır. İnce kılcal borular suya konulduğunda, su ve kılcal boru arasındaki adhezyon kuvvetleri, suyun kohezyon kuvvetlerinden büyük olduğundan su kılcal boru içerisinde yükselir. Günlük hayatta karşılaştığımız kağıt peçete ve süngerin suyu emmesi, bitkilerde suyun kökten gövde ve yapraklara iletilmesi kılcallık etkisiyledir.
Kılcal boru, cıva dolu çanağa daldırıldığında kapiler etki gözlenmez. Çünkü cıva ile kılcal boru arasındaki adhezyon kuvvetleri, cıvanın sahip olduğu kohezyon kuvvetlerinden daha küçüktür.
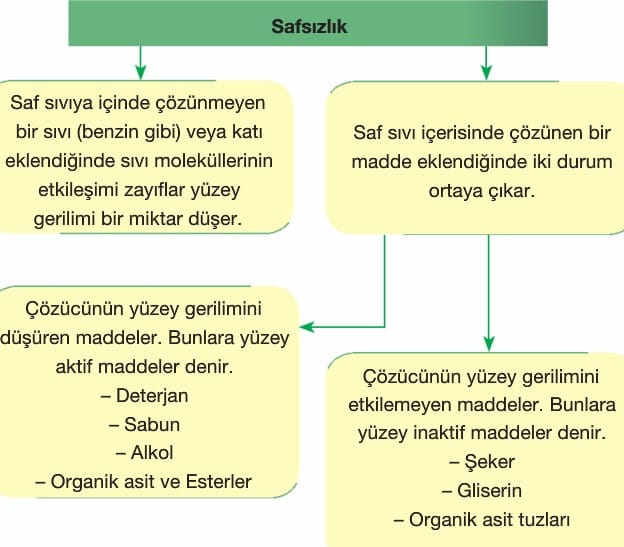
Yüzey Gerilimini Etkileyen Faktörler
1. Sıcaklık: Sıcaklık artışı, sıvı moleküllerinin kinetik enerjisini artırır, bunun sonucunda sıvı molekülleri arasında çekim kuvvetleri zayıflar ve sıvının yüzey gerilimi düşer.