Kimyasal Tepkimelerin Denkleştirilmesi 10. Sınıf Kimya
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
Kimyasal Denklemlerin Denkleştirilmesi
Bir kimyasal tepkimede atom sayısı ve cinsi kesinlikle korunur.
Buna göre, bir kimyasal denklemde bileşik ve elementlerin önüne uygun katsayılar yazılarak denklem denkleştirilir.
- * Denkleştirme yapılırken maddelerin formüllerinde hiçbir zaman değişiklik yapılmaz.
* Atom sayısı en çok olan bileşiğin katsayısı 1 alınır.
* Daha sonra bu bileşikteki atomların sayısı eşitlenir.
* Serbest halde bulunan elementler en son eşitlenir.
* Bileşikler için mümkün olduğunca tamsayı kullanılır.
* Tepkimede H ve O atomlarının olması durumunda bunların en son denkleştirilmesi daha uygundur.
kuralları kullanılarak tepkime denklemi denkleştirilir.
* En küçük tamsayılarla denkleştirme işleminde tüm maddelere tamsayı gelip gelmediği kontrol edilir. Rasyonel sayı gelen katsayı varsa tüm katsayılar iki ile genişletilerek işlem tamamlanır.
Çözümlü Örnek Test Soruları
Soru 1:
Aşağıdaki tepkimeyi denkleştiriniz:
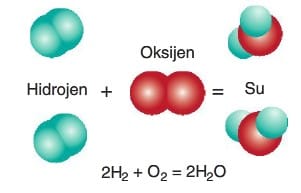
H₂ + O₂ → H₂O
A) H₂ + 2O₂ → H₂O₂
B) 2H₂ + O₂ → 2H₂O
C) H₂ + O₂ → 2H₂O
D) 2H₂ + O₂ → H₂O
E) H₂O + O₂ → H₂
Cevap:
Tepkimeyi denkleştirmek için hidrojen ve oksijen atomlarının sayısının eşit olması gerekir.
Denkleştirilmiş hali: 2H₂ + O₂ → 2H₂O
Doğru cevap: B) 2H₂ + O₂ → 2H₂O
Soru 2:
Aşağıdaki tepkimeyi denkleştiriniz:
Na + H₂O → NaOH + H₂
A) 2Na + 2H₂O → 2NaOH + H₂
B) Na + H₂O → NaOH + H₂
C) 2Na + H₂O → NaOH + H₂
D) 2Na + 2H₂O → NaOH + 2H₂
E) Na + 2H₂O → 2NaOH + H₂
Cevap:
Tepkimeyi denkleştirmek için sodyum ve hidrojen atomlarının sayısının eşit olması gerekir.
Denkleştirilmiş hali: 2Na + 2H₂O → 2NaOH + H₂
Doğru cevap: A) 2Na + 2H₂O → 2NaOH + H₂
Soru 3:
Al + O₂ → Al₂O₃ tepkimesini denkleştiriniz.
A) 4Al + 3O₂ → 2Al₂O₃
B) 2Al + 3O₂ → 2Al₂O₃
C) 4Al + O₂ → 2Al₂O₃
D) 2Al + O₂ → Al₂O₃
E) 2Al + 3O₂ → Al₂O₃
Cevap:
Tepkimeyi denkleştirmek için alüminyum ve oksijen atomlarının sayısını eşitlemek gerekir.
Denkleştirilmiş hali: 4Al + 3O₂ → 2Al₂O₃
Doğru cevap: A) 4Al + 3O₂ → 2Al₂O₃
Soru 4:
Aşağıdaki tepkimeyi denkleştiriniz:
C₃H₈ + O₂ → CO₂ + H₂O
A) C₃H₈ + 5O₂ → 3CO₂ + 4H₂O
B) C₃H₈ + 4O₂ → 3CO₂ + 4H₂O
C) C₃H₈ + 5O₂ → 3CO + 4H₂O
D) C₃H₈ + O₂ → CO₂ + H₂O
E) C₃H₈ + 6O₂ → 3CO₂ + H₂O
Cevap:
Tepkimeyi denkleştirmek için karbon, hidrojen ve oksijen atomlarının sayısını eşitlemeliyiz.
Denkleştirilmiş hali: C₃H₈ + 5O₂ → 3CO₂ + 4H₂O
Doğru cevap: A) C₃H₈ + 5O₂ → 3CO₂ + 4H₂O
Soru 5:
Mg + HCl → MgCl₂ + H₂ tepkimesini denkleştiriniz.
A) Mg + HCl → MgCl₂ + H₂
B) Mg + 2HCl → MgCl₂ + H₂
C) Mg + HCl₂ → MgCl₂ + H₂
D) 2Mg + HCl → MgCl₂ + H₂
E) 2Mg + 2HCl → 2MgCl₂ + H₂
Cevap:
Tepkimeyi denkleştirmek için hidrojen ve klor atomlarının sayısını eşitlememiz gerekir.
Denkleştirilmiş hali: Mg + 2HCl → MgCl₂ + H₂
Doğru cevap: B) Mg + 2HCl → MgCl₂ + H₂
Soru 6:
Fe + O₂ → Fe₂O₃ tepkimesini denkleştiriniz.
A) Fe + O₂ → Fe₂O₃
B) 2Fe + 3O₂ → 2Fe₂O₃
C) 4Fe + 3O₂ → 2Fe₂O₃
D) 2Fe + O₂ → Fe₂O₃
E) Fe + 2O₂ → Fe₂O₃
Cevap:
Tepkimeyi denkleştirmek için demir ve oksijen atomlarının sayısını eşitlemek gerekir.
Denkleştirilmiş hali: 4Fe + 3O₂ → 2Fe₂O₃
Doğru cevap: C) 4Fe + 3O₂ → 2Fe₂O₃
Soru 7:
Ca + H₂O → Ca(OH)₂ + H₂ tepkimesini denkleştiriniz.
A) Ca + 2H₂O → Ca(OH)₂ + H₂
B) Ca + H₂O → Ca(OH)₂ + H₂
C) 2Ca + H₂O → 2Ca(OH)₂ + H₂
D) Ca + H₂O₂ → Ca(OH)₂ + H₂
E) Ca + H₂O → CaO + H₂
Cevap:
Tepkimeyi denkleştirmek için hidrojen atomlarının sayısını eşitlemeliyiz.
Denkleştirilmiş hali: Ca + 2H₂O → Ca(OH)₂ + H₂
Doğru cevap: A) Ca + 2H₂O → Ca(OH)₂ + H₂
Soru 8:
N₂ + H₂ → NH₃ tepkimesini denkleştiriniz.
A) N₂ + 3H₂ → 2NH₃
B) 2N₂ + H₂ → NH₃
C) N₂ + H₂ → 2NH₃
D) N₂ + 2H₂ → 2NH₃
E) 2N₂ + 3H₂ → 2NH₃
Cevap:
Azot ve hidrojen atomlarının sayısını eşitlemeliyiz.
Denkleştirilmiş hali: N₂ + 3H₂ → 2NH₃
Doğru cevap: A) N₂ + 3H₂ → 2NH₃
hiç bir şey anlamadım daha iyi anlatabilirsiniz
desem yalan olur çok güzel anlatmışsıız
cok tesekkur ederim odevimi yapabildim