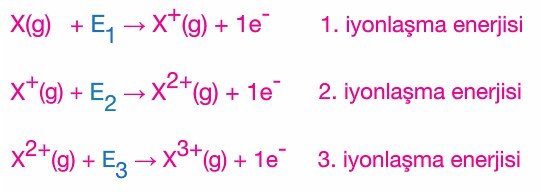İyonlaşma Enerjisi Nedir? 9.Sınıf Kimya
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
- Gaz haldeki bir atomdan bir elektron koparmak için verilmesi gereken enerji miktarıdır.
- E3 > E2 > E1 ( E–> elektron koparmak için verilen enerji miktarını temsil eder.)
- Atomun kaç elektronu varsa o kadar sayıda iyonlaşma enerjisi vardır.
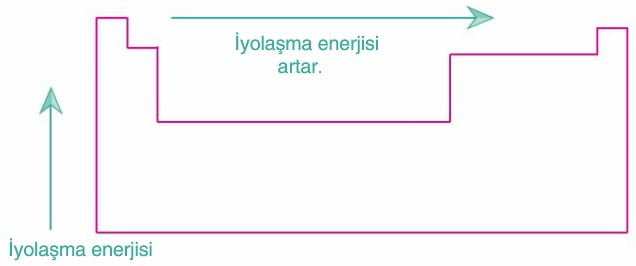
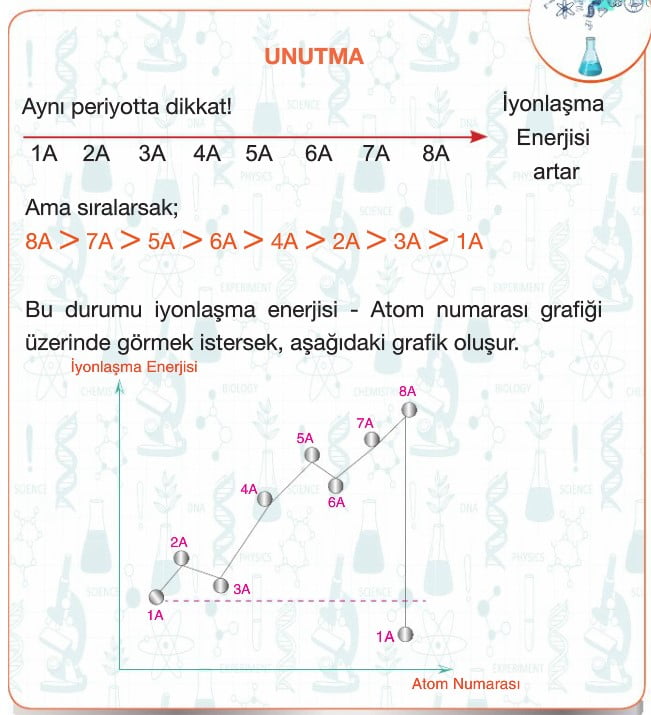
- Kısaca, iyonlaşma enerjisi He’ye doğru artar.
İyonlaşma Enerjisi konu anlatımı ders notu çözümlü örnekler 9.sınıf kimya
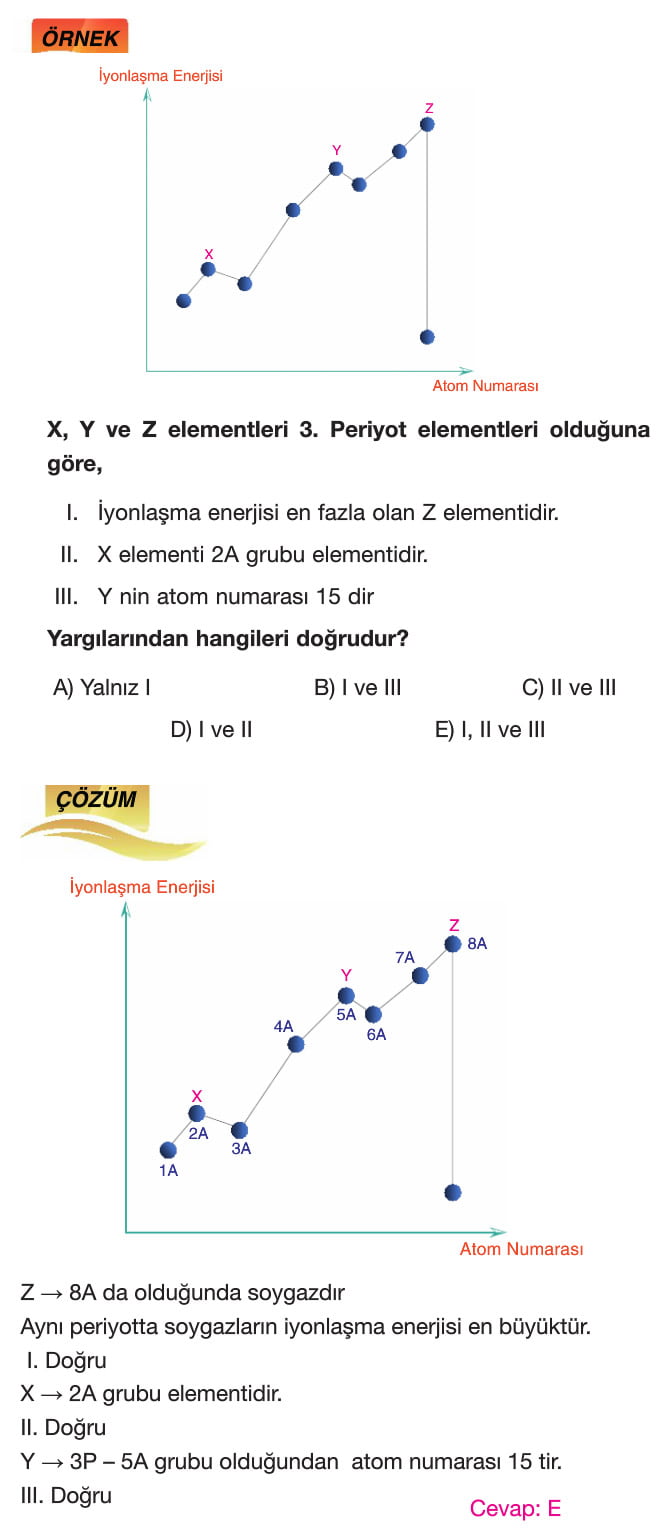
Örnek: x, y, z elementleri 3. periyotta olduğuna göre;
I. iyonlaşma enerjisi en fazla olan Z elementidir.
II. X elementi 2A grubu elementidir.
III. Y nin atom numarası 15 dir.
Yargılarından hangileri doğrudur.
Çözüm: Z elementi 8A grubunda olduğundan dolayı soygazdır. Aynı periyotta soygazların iyonlaşma enerjisi en büyüktür. Yani I. madde doğrudur.
X elementi 2A grubunda olduğundan dolayı II. madde de doğrudur.
Y elementi 3P - 5A grubu elementi olduğundan dolayı atom numarası 15 tir. III. madde de doğrudur. Dolayısıyla doğru cevap E şıkkıdır.
Çözüm 2: İyonlaşma enerjisi, gaz haldeki nötr atoma enerji vererek elektron koparma olayı 1. iyonlaşma enerjisidir.