Isı, Sıcaklık, Öz Isı 8.Sınıf Fen
🪄 Test ve Çalışma Kağıdı Hazırla
Konunu yaz; MEB uyumlu test ve özetler saniyeler içinde hazırlansın. 🖨️ Ücretsiz PDF indir!
Isı ve sıcaklık, günlük hayatımızda çok yaygın olarak kullandığımız sözcüklerdir. “Hava bugün çok sıcak?, “Bu oda çok ısındı.”, “Su ısındı.”, “Hava ısındı.” gibi. Maddeler katı, sıvı ve gaz olmak üzere üç ayrı fiziksel hâlde bulunurlar. Bütün maddeler atom ve moleküllerden (taneciklerden) oluşur. Bu tanecikler sürekli hareket hâlindedir. Hareket halindeki bu taneciklerin kinetik enerjisi de artar. Katı haldeki maddelerin tanecikleri sadece titreşim hareketi yaparken, sıvı ve gaz halindeki maddelerin tanecikleri sürekli titreşim ve yer değiştirme hareketi yapar. Taneciklerin tek tek sahip oldukları kinetik enerji değeri hissedilmeyecek kadar azdır. Bir maddedeki taneciklerin kinetik enerjilerinin toplamına ısı enerjisi denir.
Bir maddedeki taneciklerin tümünün sahip olduğu kinetik enerjileri toplamı (ısı enerjisi), toplam tanecik sayısına bölünürse tanecik başına düşen ortalama bir değer bulunur. Bir maddede tanecik başına düşen ortalama kinetik enerji ile orantılı olan bu değere sıcaklık denir. Isı ve sıcaklık kavramları birbirinden farklı olmasına karşın aralarında bir ilişki vardır. Bir cisim çevresinden ısı aldığında veya çevresine ısı verdiğinde sıcaklığı değişir. Maddelere ısı verildiğinde tanecikleri hızlanır ve kinetik enerjileri artar. Isı enerjisi kazanan maddelerin sıcaklığı yükselir. Maddeler ısı kaybettiğinde tanecikleri yavaşlar ve kinetik enerjileri azalır. Isı kaybeden maddelerin sıcaklığı azalır.
Isı Kavramı (Q)
“Çaydanlıktaki su ısındı.”
“Öğle oldu hava ısındı.”
“Uzun süre yanan lamba çok ısındı.”
“Taş kömürünün verdiği ısı çok büyüktür.”
gibi ifadeler ısıyı ve ısı ile madde etkileşimini ifade eder. Bir maddenin ısısı denildiğinde, o maddeyi oluşturan taneciklerin hareket (kinetik) enerjilerinin ve potansiyel enerjilerinin (moleküller arası bağ enerjisi) toplam büyüklüğü anlaşılır. Isı bir maddenin bütün moleküllerinin toplam kinetik ve potansiyel enerjisidir. Isı bir enerji türüdür. Q harfi ile ifade edilir. Birimleri; joule (J) veya kalori (cal) dir. Isı enerjisi her maddenin taşıdığı bir enerji türüdür. Kütlesi ve belirli sıcaklığı olan her madde ısı enerjisine sahiptir.
Sıcaklık Kavramı (t)
Sıcaklık maddeyi oluşturan moleküllerden birinin sahip olduğu ortalama hareket enerjisinin büyüklüğünü ifade eden bir ölçüm değeridir. Sıcaklık maddede molekül başına düşen ortalama hareket enerjisinin büyüklüğünü ifade eden bir tanımlamadır. “Bugün hava çok sıcak.” dediğimizde etrafımızı kaplayan hava moleküllerinin büyük bir hareket enerjisine sahip olduğunu ifade etmiş oluruz. Sıcaklık bir enerji olmayıp, enerji ile ilgili bir büyüklük ifadesidir. Termometre aracı ile doğrudan ölçülebilen skaler bir büyüklüktür. sıcaklığın artması demek, madde moleküllerinin ortalama hareket enerjilerinin artması demektir.
“Yanan bir kibrit çöpünün sıcaklığı mı, yoksa şu ormanın sıcaklığı mı daha büyüktür?” gibi bir soru karşısında; elbette ki yanan kibrit çöpünün sıcaklığı daha yüksektir cevabını vermeliyiz. Çünkü yanan kibrit çöpünde tek molekülün hareket enerjisi, ormandaki ağaçları oluşturan moleküllerin enerjisinden daha büyük olacaktır. Kibrit çöpüyle ormanın sahip olduğu ısılar karşılaştırıldığında ise, ormanın sahip olduğu ısı enerjisinin daha büyük olduğunu söyleriz. Çünkü, ormanı oluşturan madde molekülü çok fazladır. Bu sebeple ormanın sahip olduğu toplam kinetik enerji, kibrit çöpünün sahip olduğu enerjiden daha büyüktür. Isı ve sıcaklık farklı kavramlardır.
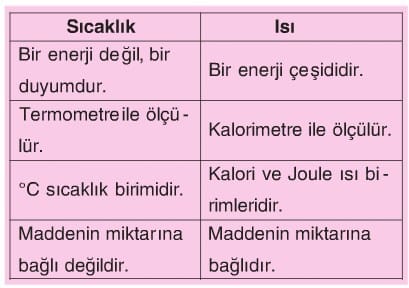
Sıcaklık ve Isı Arasındaki Farklar
Isı Alışverişi
- Sıcaklıkları farklı olan iki madde, Isıca yalıtılmış bir ortamda bir araya getirilirse aralarında ısı alışverişi olur.
- Sıcaklığı fazla olan maddeden, sıcaklığı düşük olan maddeye ısı enerjisi geçer. Maddelerin son sıcaklıkları eşit oluncaya kadar ısı alışverişi devam eder.
- Isıca yalıtılmış ortamda maddelerin ısı enerjilerindeki değişimler eşit olur.
Qalınan = Qverilen
Sıcaklığın Ölçülmesi
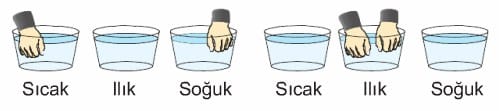
Maddelerin hangisinin sıcak, hangisinin soğuk olduğunu dokunarak anlayabiliriz. Ancak dokunma duyumuzla sıcaklığı ölçemediğimiz gibi kıyaslamasında da yanılabiliriz.
Sıcak ve soğuk suda bulunan parmaklarını ılık suya sokan Hasan şaşırır. Çünkü sıcak sudan getirdiği parmağı ile ılık suyu soğuk olarak algılarken, soğuk sudan getirdiği parmaklarını da sıcak olarak algılar. Sıcaklığı sayısal olarak ölçmeye yarayan cihazlara termometre denir. Bir maddenin sıcaklığı termometre ile doğrudan ölçülebilir. Termometreler, maddelerin sıcaklığına bağlı olarak genleşme özelliğinden faydalanılarak geliştirilmiştir. Bir termometrenin ölçebileceği sıcaklık aralığı, termometrenin yapımında kullanılan sıvının donma ve kaynama sıcaklıkları arasında bir değerdir.
Kütle – Sıcaklık İlişkileri
Isı, maddeler üzerinde sıcaklık değişimine neden olabilir. Isı enerjisi aktarılan bir maddenin sıcaklığı artabilir.
- Bir maddenin aldığı ısı enerjisi, maddenin miktarına bağlıdır.
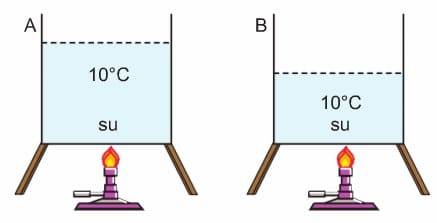
A ve B kaplarında sıcaklıkları 10 °C olan sular vardır. Suları özdeş ısı kaynaklarının üstüne koyalım ve suları kaynatmaya çalışalım.
A kabındaki suyun kaynayabilmesi için, bu kabın B kabından daha uzun süre ısı kaynağının üzerinde kalması gerekir. Yani daha fazla enerjiye ihtiyaç duyulur. Bunun nedeni A kabındaki su miktarının B kabındakine göre daha fazla olmasıdır. Bir maddenin kütlesi arttıkça, o maddeyi belli bir sıcaklığa ulaştırmak için daha fazla ısı enerjisine ihtiyaç duyulur. İçlerinde farklı miktarlarda su bulunan A ve B kaplarında sıcaklıkları 10 °C olan sular özdeş ısı kaynaklarının üstünde, eşit süre ısıtalım.
Bu sürenin sonunda A ve B kaplarındaki suların son sıcaklıklarını karşılaştırdığımızda, B kabındaki suyun sıcaklığının A kabındaki suyun sıcaklığından fazla olduğunu görürüz. Örneğin, A kabındaki suyun son sıcaklığı 50 °C olarak ölçülürken, B kabındaki suyun son sıcaklığı 80 °C olarak ölçülebilir. Bir maddenin kütlesi arttıkça, o maddeye verilen ısı enerjisinin, maddenin sıcaklığında sebep olduğu değişme daha az olur.
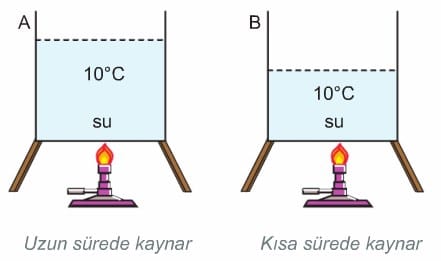
Isı miktarının sıcaklık değişimine etkisi
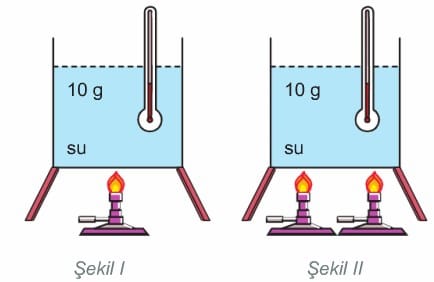
Bir maddenin eşit miktarlarına farklı miktarda ısı verildiğinde fazla ısı verilen kaptaki maddenin sıcaklığındaki değişme daha fazla olur. Şekil II’deki kapta bulunan su, Şekil I’deki kaptaki suya göre daha erken kaynamaya başlar. Buna göre, sıcaklık değişiminin verilen ısı miktarıyla doğru orantılı olduğu sonucuna ulaşılabilir. Kısaca sıcaklık değişiminin (ΔT), kütle (m) ve özısı (c) ile ters, ısı miktarıyla (Q) doğru orantılı olduğu sonucuna varılır.
Öz Isı
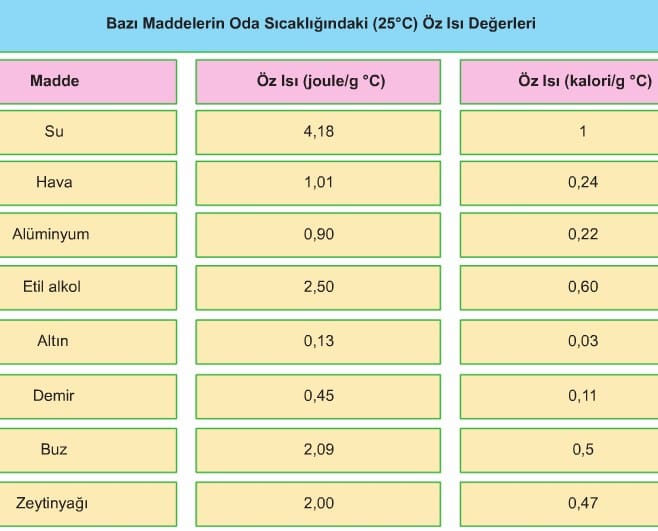
1 gram maddenin sıcaklığını 1°C arttırmak için gerekli ısı miktarına öz ısı adı verilir. Öz ısı kısaca “c” sembolü ile gösterilir, birimi J/g °C’tur. Her maddenin öz ısısı farklı olup öz ısı ayırt edici bir özelliktir. Bir maddenin aldığı veya verdiği ısı miktarı, kütlesine ve cinsine (öz ısısına) bağlı olarak değişir. Bazı maddelerin oda sıcaklıklarındaki öz ısı değerleri aşağıdaki tabloda verilmiştir.

Çok teşekkür ederim! Şu anda sınavlara hazırlanıyorum ve bu bana çok yardımcı oldu!